10.3. Первичные процессы при действии ионизирующих излучений
При облучении биологических объектов, содержащих воду, находящуюся частично в свободном состоянии, а частично входящую в состав органелл соответствующих биосистем, принято считать, что 50% поглощенной дозы в «средней» клетке приходится на воду, другие 50% — на ее органеллы и растворенные вещества. В соответствии с локализацией поглощенной энергии (в воде или в основном веществе) можно говорить о непрямом и прямом действии ионизирующего излучения.
При взаимодействии ионизирующего излучения с водой в конечном итоге происходит выбивание электронов из молекул воды с образованием так называемых молекулярных ионов, несущих положительный и отрицательный заряд. Схематически этот процесс можно представить следующим образом:
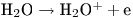
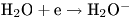
Возникающие ионы воды в свою очередь распадаются с образованием ряда радикалов, которые взаимодействуют между собой:
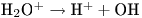
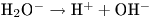
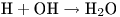
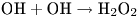
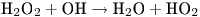
Считается, что основной эффект лучевого воздействия обусловлен такими радикалами, как 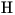 ,
, 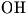 и особенно
и особенно 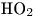 (гидропероксид). Последний, радикал, обладающий высокой окислительной способностью, образуется при облучении воды в присутствии кислорода:
(гидропероксид). Последний, радикал, обладающий высокой окислительной способностью, образуется при облучении воды в присутствии кислорода: 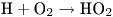 . Выход этого радикала уменьшается пропорционально падению парциального давления кислорода. Этим объясняется кислородный эффект при облучении, проявляющийся в том, что при снижении концентрации кислорода в период облучения уменьшается эффект лучевого воздействия.
. Выход этого радикала уменьшается пропорционально падению парциального давления кислорода. Этим объясняется кислородный эффект при облучении, проявляющийся в том, что при снижении концентрации кислорода в период облучения уменьшается эффект лучевого воздействия.
Кислородный эффект отсутствует при облучении биообъектов излучением с высоким значением ЛПЭ (например, нейтронами). Это явление объясняется тем обстоятельством, что при взаимодействии частиц с веществом создается высокая удельная концентрация радикалов 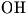 , при которой протекают следующие реакции:
, при которой протекают следующие реакции:
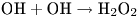
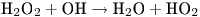
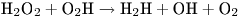
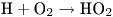
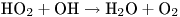
Таким образом, в этом случае кислород, необходимый для возникновения радикала 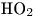 , продуцируется непосредственно в зоне поглощения энергии, поэтому количество возникающих в данном случае окислительных радикалов не зависит от степени насыщенности растворов кислородом.
, продуцируется непосредственно в зоне поглощения энергии, поэтому количество возникающих в данном случае окислительных радикалов не зависит от степени насыщенности растворов кислородом.
Возникшие в результате взаимодействия излучений с водой радикалы взаимодействуют с растворенными молекулами различных соединений, давая начало вторично-радикальным продуктам. Время жизни этих продуктов значительно больше по сравнению со сроком жизни первичных радикалов, поэтому для них возможно проявление большей «избирательности» действия.
Пути размена энергии при действии ионизирующих излучений могут быть представлены на первом этапе возникновением ионизованных и возбужденных молекул.
Важнейшими процессами, ведущими к химическим преобразованиям (а следовательно, к поражению) биомолекул, являются:
- диссоциации возбужденных молекул на соответствующие молекулярные продукты;
- взаимодействие с сенсибилизатором (например,
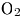 ).
).
Кроме указанных механизмов размена энергии, возможны:
- процесс переноса энергии возбуждения путем реабсорбции (перепоглощения активатором света люминесценции растворителя),
- образование комплексов молекул растворителя и активатора с передачей энергии внутри этого комплекса, передачей энергии при столкновении (диффузионный механизм) и др.
Конкурировать с перечисленными процессами поражения могут эффекты восстановления, к которым относятся люминесценция и преобразование энергии возбуждения в тепло.
Важно подчеркнуть, что в результате прямого и непрямого действия ионизирующих излучений на биосубстрат возникают идентичные «вторичные» радикалы, которые могут служить объяснением определенной специфичности радиационно-химических превращении.
Дальнейшие этапы развития радиационного поражения молекулярных структур и наиболее радиочувствительных надмолекулярных образований сводятся к изменениям белков, липидов и углеводов. Так, например, облучение белковых растворов приводит к конфигурационным изменениям белковой структуры, агрегации молекул за счет образования дисульфидных связей, деструкции, связанной с разрывом пептидных или углеродных связей. Все эти процессы наблюдаются при поглощении достаточно высоких доз — порядка сотен тысяч рад и более. При облучении целостного организма в первую очередь изменяется содержание свободных аминокислот в тканях.
При общем облучении экспериментальных животных дозой 5 Гр (500 рад) понижается уровень метионина (важнейшего донора метильных групп) на 75%, триптофана — на 26%. Эти изменения оказывают большое влияние на белковый обмен, поскольку недостаток хотя бы одной аминокислоты приводит к резкому замедлению биосинтеза белков. Отмечаемое уменьшение содержания сульфгидрильных групп в тканях облученных животных относится к наиболее ранним радиационным изменениям. В дальнейшем оно прогрессирует и достигает более 50% по отношению к исходному уровню на 5-е сутки при облучении дозой 6 Гр (600 рад). Считается, что начальная инактивация сульфгидрильных групп вызывается короткоживущими радикалами, а в дальнейшем она происходит за счет действия стойких перекисей.
Различные ферментные системы реагируют на облучение неоднозначно. Активность одних ферментов после облучения возрастает, других понижается, третьих остается неизменной. Важно отметить, что при облучении организма происходят повреждение систем синтеза нуклеиновых кислот и стимуляция ферментативных систем, деполяризующих эти макромолекулы.
К числу наиболее радиочувствительных процессов в клетке относится окислительное фосфорилирование. Нарушение этого процесса отмечается уже через несколько десятков минут после облучения дозой 1 Гр (100 рад). Оно проявляется в повреждении системы генерирования АТФ, без которого не обходится ни один процесс жизнедеятельности. Высокой чувствительностью обладают дезоксирибонуклеиновые комплексы (ДНК клеточного ядра, в комплексе со щелочными белками, РНК и ферментами). Уже через несколько минут после облучения имеет место высвобождение нуклеиновой кислоты из дезоксинуклео-протеида (ДНП) и одновременное накопление нуклеиновых кислот в цитоплазме облученных клеток. Предполагается, что в этом случае в первую очередь поражаются связи белок-белок и белок — ДНК.
Облучение простых сахаров значительными дозами приводит к их окислению и распаду, в результате чего образуются органические кислоты и формальдегид. Облучение растворов полисахаридов (например, крахмала) сопровождается значительным понижением их вязкости, появлением простых сахаров (глюкозы, мальтозы) и др.
При дозах порядка 5 — 10 Гр (500 — 1000 рад) выявлены изменения в мукополисахаридах. Так, понижается вязкость гиалуроновой кислоты, теряется ее способность к соединению с белком. Облучение другого мукополиса-харида — гепарина — приводит к его деполяризации, которая сопровождается потерей антикоагулянтных свойств. При облучении целостного организма происходит понижение содержания гликогена в скелетных мышцах, печени и ряде других тканей, как предполагают, в результате нейрогуморальной реакции на облучение. Кроме того, обнаруживается нарушение процессов распада глюкозы и в первую очередь — анаэробного гликолиза.
При действии ионизирующих излучений на липиды происходит образование перекисей, которым придают особо важное значение в развитии лучевого поражения.
При облучении организма отмечается снижение содержания липидов и их перераспределение в различных тканях с повышением их уровня в печени и крови, что, по-видимому, связано с изменениями углеводного обмена. Наряду с некоторой стимуляцией синтеза липидов происходит также повышенная их окисляемость, в результате которой возникают перекиси. При этом образование перекисей обусловлено не столько прямым действием радиации, сколько результатом угнетения ряда антиоксидантов.
Перечисленные выше некоторые поражения молекулярных структур, возникающие в результате облучения, далеко не исчерпывают все сведения, которые накоплены к настоящему времени в этой области. Вместе с тем эта информация до настоящего времени пока еще носит описательный, качественный характер.